Химики нашли удобный способ окисления белого фосфора

Химики из Германии научились легко превращать белый фосфор в удобный исходник для синтеза фосфорорганических соединений. Реакция фосфора с окислителем и основанием привела к образованию соли, катион которой содержал один атом фосфора. Как пишут химики в Nature Chemistry, ее удалось превратить в замещенные фосфины, фосфиты и фосфористую кислоту.
В промышленности фосфор получают из минералов — апатитов и фосфоритов. Их либо обрабатывают серной кислотой, чтобы получить фосфорную кислоту, либо электрохимически восстанавливают до белого фосфора. Далее белый фосфор хлорируют, а из трихлорида PCl3 получают фосфорорганику. Например, реакции PCl3 с магнийорганическими соединениями приводят к тризамещенным органическим фосфинам PR3.
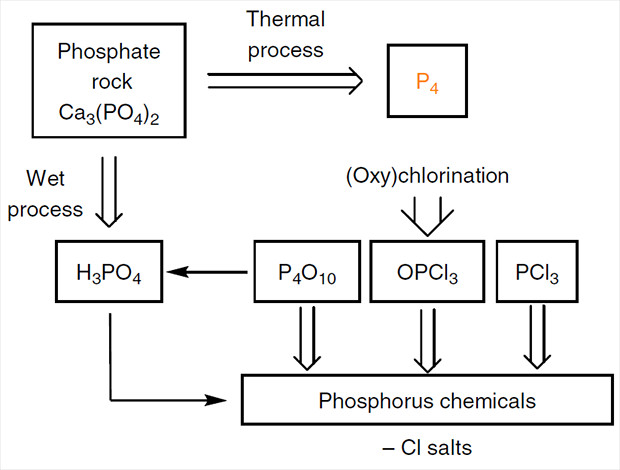
Часто реакции замещения атомов хлора в PCl3 протекают неселективно. А сам трихлорид фосфора — неудобный исходник: он ядовитый, и получают его с помощью хлора — токсичного удушающего газа. Поэтому ученые пытаются заменить стадию хлорирования более удобным превращением.
