GMP-вызов для животноводов
Что изменилось на рынке ветпрепаратов после того, как новые правила сертификации стали обязательными для всех производителей

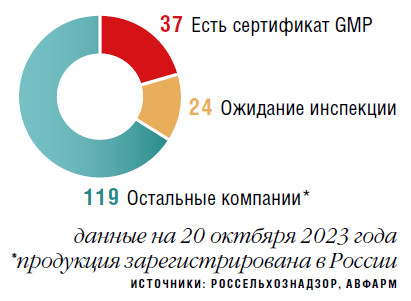
Вопреки опасениям, массового дефицита импортных ветпрепаратов после вступления в силу требований соответствию нормам GMP не возникло благодаря заранее сформированным запасам препаратов. Однако из примерно 180 иностранных площадок, продукция которых зарегистрирована в России и ЕАЭС, действующие заключения GMP пока имеют лишь 37, и как изменится ситуация после исчерпания запасов — непонятно. Впрочем, внутреннее производство растет , и уход, пусть даже временный, зарубежных игроков дает возможность российским предприятиям увеличить свою долю рынка.
С 1 сентября производители ветеринарных фармацевтических препаратов должны иметь положительное заключение о соответствии требованиям правил GMP в России (ЕАЭС). Продукция зарубежных компаний, не прошедших проверку, не может поставляться в страну. Как уточнял Россельхознадзор, эта норма «направлена исключительно на унификацию требований к российским и иностранным производителям ветеринарных препаратов». Все российские компании обязаны получать заключения о соответствии требованиям GMP, тогда как иностранные должны были оформлять его только на те препараты, которые были зарегистрированы уже после внедрения стандарта GMP в России.
Летом Ассоциация ветеринарных фармацевтических компаний (АВФАРМ) предупреждала, что это может привести к резкому сокращению количества импортных ветеринарных препаратов на российском рынке, поскольку далеко не все иностранные производители успеют пройти инспекции. Среди причин назывались не до конца стандартизированные требования и разные подходы со стороны инспекторов. Правда, за более чем полтора месяца действия новой нормы она фактически не повлияла на отрасль, поскольку участники рынка заранее сформировали запасы ветпрепаратов, которые могли стать дефицитом. Сельхозпроизводители отмечают отсутствие некоторых привычных средств, в частности вакцин, но причиной этого могут быть другие факторы.
Нюансы сертификации
Наряду с международными нормами, как в российском, так и евразийском законодательстве с 2017 года предусмотрено инспектирование производственных площадок на соответствие GMP-требованиям, однако часть зарубежных производителей за семь лет так и не привела свою деятельность в соответствие меняющемуся российскому законодательству. При этом еще до 1 сентября 2023-го, а фактически с первой половины 2022 года, некоторые крупные иностранные компаний по собственной инициативе значительно снизили, а в ряде случаев вообще прекратили поставки отдельных позиций производимой продукции на российский рынок, сообщили «Агроинвестору» в пресс-службе Россельхознадзора.
По данным ведомства, на начало третьей декады октября 37 зарубежных площадок, производящих лекарственные препараты для ветеринарного использования, имели действующие заключения GMP, 24 площадки находились в ожидании инспектирования. «Мы не ждем, что такую сертификацию пройдут все 180 площадок, продукция которых зарегистрирована в России и в других юрисдикциях ЕАЭС, но пока число сертифицированных производителей критически мало, — подчеркивает исполнительный директор АВФАРМ Семен Жаворонков. — Как мы не раз отмечали, текущее состояние аттестации зарубежных предприятий не позволяет говорить о стабильности обеспечения российских потребителей, в том числе аграриев, востребованными ветпрепаратами в необходимых объемах и ассортименте».
По его словам, в сентябре в гражданский оборот не было введено ни одной серии ветпрепаратов зарубежного производства. В октябре было введено нескольких первых серий химико-фармацевтических препаратов зарубежного производства, главным образом антибиотиков, вакцин среди них пока нет. «Те позиции, которые аналитики видят в продажах сегодня, — это реализация запасов, сформированных участниками дистрибьюторской сети из продукции, ввезенной до вступления новых требований в силу», — поясняет Жаворонков.
О том, что с сентября изменятся условия доступа на российский рынок ветпрепаратов, все компании знали, и, естественно, до наступления этой даты они старались сформировать запас продукции с тем расчетом, чтобы с его помощью можно было относительно безболезненно пройти переходный период, подтверждает директор по развитию аналитической компании «АРЭНСИ Фарма» Николай Беспалов. Активность по формированию запасов стартовала еще в июле 2023-го: там хорошо виден пик поставок (в 2,5–3 раза больше обычных значений), который для данного сезона совершенно нехарактерен, говорит он. «В принципе, тех объемов препаратов, которые сейчас сконцентрированы на складах, в теории должно хватить на три-четыре месяца нормальной работы, так что с точки зрения доступности импортных препаратов до конца текущего года глобальных перебоев быть не должно, — рассуждает эксперт. — Хотя в долгосрочном периоде, конечно, возможны разные сценарии, в том числе ряд компаний может отказаться от поставок или не сможет вовремя получить необходимые документы, но эти последствия мы в полной мере сможем наблюдать только в начале будущего года». По сведениям Россельхознадзора, запасов зарубежной продукции, которая ввозилась в Россию до 1 сентября, должно хватить на период 1–1,5 лет.
Многие дистрибьюторы сформировали запасы, это ясно отражает статистика ввоза в этом и прошлом году, соглашается Жаворонков. Аналогично поступили и крупные холдинги, у которых есть возможности закупать и продолжительное время хранить с соблюдением всех требований большие объемы ветпрепаратов. Глава Национальной мясной ассоциации (НМА) Сергей Юшин отмечает, что большое количество необходимых импортных ветеринарных препаратов в нашу страну по-прежнему поступает, хотя у некоторых птицеводов есть сложности с вакцинами. «Есть компании, которые, опасаясь дефицита ветпрепаратов в преддверии вступления в силу правил сертификации по GMP, закупали их на полгода — девять месяцев вперед, и они сейчас обеспечены необходимыми препаратами», — знает он. Предприятия молочной отрасли имеют определенные запасы ветпрепаратов, что позволяет либо постепенно перейти на российские аналоги, либо дождаться получения GMP иностранными поставщиками, которые пока не смогли этого сделать, говорит гендиректор Национального союза производителей молока (Союзмолоко) Артем Белов.
В перспективе риск сокращения предложения на более чем 500 наименований, безусловно, негативно повлияет на рыночную конкуренцию, предупреждает Жаворонков. «Нельзя так резко закрыть рынок для по-настоящему востребованных препаратов и рассчитывать, что потребители вдруг обнаружат действительно конкурентоспособные альтернативы, которых почему-то не замечали ранее», — уверен он.

При этом успешная сертификация остается приоритетной целью производителей ветпрепаратов, входящих в АВФАРМ, продолжает Жаворонков. «При этом мы хорошо понимаем, что прохождение российской GMP-инспекции — продолжительный процесс, который с точки зрения статистики чаще не приводит к получению необходимого сертификата, — рассказывает он. — С 2017 года отечественные инспекторы провели 191 инспекцию, но только в 42 % случаев признали предприятия соответствующими требованиям. При этом есть примеры предприятий, которые инспекторы за это время проверили уже три и четыре раза, но они не получили нужных сертификатов GMP. В целом на предприятиях наших участников из 65 инспекций 76 % завершились отказами в выдаче российских сертификатов».
По словам Жаворонкова, российский сертификат GMP действует три года, а процесс его получения с момента подачи заявки на инспектирование занимает около года. Если по каким-то причинам инспекция завершается неудачно и для соблюдения требований необходимы изменения в процессах производства или контроля, то следующая инспекция откладывается. «Речь идет не только о трех месяцах, которые установлены российским законодательством на устранение замечаний, но и о мероприятиях, которые требуют больше времени. На практике редко когда повторная инспекция возможна раньше, чем через один-два года после неудачной предшествующей», — добавляет глава АВФАРМ.
Сейчас участники Ассоциации — компании Boehringer Ingelheim, MSD Animal Health и Zoetis — продолжают принимать запланированные российские инспекции и устранять замечания, выявленные по итогам уже состоявшихся проверок. АВФАРМ, в свою очередь, предпринимает усилия, чтобы совместно с регулятором выработать решение, позволяющее оптимизировать процесс инспектирования и получения сертификатов. «Убеждены, что правила надлежащей производственной практики — это стандартная, повсеместно принятая процедура, которая должна работать для защиты потребителей и ни в коем случае не должна становиться препятствием для доступа на рынок качественной продукции, востребованной и широко используемой в десятках стран», — отмечает Жаворонков.
Сертификат GMP есть лишь у каждого пятого зарубежного производителя